中國上海和香港2021年4月13日 /美通社/ -- 致力於研發和商業化創新腫瘤療法的生物制藥公司—德琪醫藥有限公司(簡稱"德琪醫藥",6996.HK)宣布,公司於2021年美國癌症研究學會(AACR)年會上公布ATG-010 (selinexor, XPO1抑制劑)聯合ATG-008(onatasertib, mTORC1/2抑制劑)治療三重打擊彌漫性大B細胞淋巴瘤(DLBCL)協同效果的臨床前數據。
試驗結果顯示,ATG-010聯合ATG-008在體內體外均體現出抗腫瘤和協同作用,在三重打擊彌漫性大B細胞淋巴瘤細胞株中也具有強大的協同性。同時,在DLBCL異種腫瘤移植模型中,ATG-010和ATG-008的聯合治療同樣增強了對腫瘤生長的抑制效果,顯示出協同的抗腫瘤作用。
ATG-010是一款單藥口服XPO1抑制劑,也是同類首款且唯一一款選擇性核輸出抑制劑(SINE),已被美國食品藥品監督管理局(FDA)批准治療二線以上的彌漫性大B細胞淋巴瘤患者。ATG-008是一款mTORC1/2雙靶點抑制劑,根據臨床前及臨床試驗數據,ATG-008對彌漫性大B細胞淋巴瘤有抑制作用。德琪醫藥正在開展一項ATG-010聯合ATG-008治療難治復發性彌漫性大B細胞淋巴瘤的臨床試驗(MATCH)。
臨床前數據顯示:
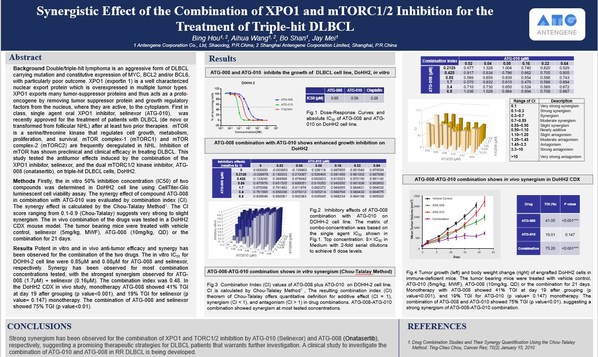
- ATG-008、ATG-010在體外均對彌漫性大B細胞淋巴瘤細胞株的生長有抑制作用。
- ATG-008聯合ATG-010增強了對三重打擊彌漫性大B細胞淋巴瘤生長的抑制作用。
- ATG-008聯合ATG-010在體外對三重打擊彌漫性大B細胞淋巴瘤具有協同的抑制作用。
- ATG-008聯合ATG-010在體內對三重打擊彌漫性大B細胞淋巴瘤細胞株的異種移植腫瘤模型具有協同的抑制作用。
德琪醫藥創始人、董事長兼首席執行官梅建明博士表示:「ATG-010已經獲批治療難治復發性彌漫性大B細胞瘤,而ATG-008對該瘤種也顯示出了臨床活性。通過對體外及體內DLBCL模型的評估,我們發現一定濃度下的ATG-010與ATG-008聯合,在三重打擊DLBCL中達到了1+1>2的腫瘤抑制效果。ATG-008與ATG-010強大的協同作用,對DLBCL患者的治療顯示出一定的應用前景,包括對有巨大臨床需求的三重打擊疾病。我們將通過MATCH試驗繼續發掘該聯合方案的臨床潛力。」
關於德琪醫藥
德琪醫藥有限公司(簡稱"德琪醫藥",香港聯交所股票代碼:6996.HK)是一家以研發為驅動的生物制藥領先企業,致力於為亞太乃至全球患者提供最領先的療法,治療腫瘤及其他危及生命的疾病。自2017年正式運營以來,德琪醫藥通過合作引進和自主研發,建立了一條從臨床前到臨床階段的不斷延展的豐富產品管線。目前,德琪醫藥已在多個亞太市場獲得13個臨床批件(IND),並遞交了5個新藥上市申請(NDA)。德琪醫藥將以"醫者無疆,創新永續"為願景,專注於同類首款和同類最優療法的早期研發、臨床研究、藥物生產及商業化,解決亟待滿足的臨床需求。欲了解更多,請訪問:www.antengene.com。
前瞻性聲明
本文所作出的前瞻性陳述僅與本文作出該陳述當日的事件或資料有關。除法律規定外,於作出前瞻性陳述當日之後,無論是否出現新資料、未來事件或其他情況,我們並無責任更新或公開修改任何前瞻性陳述及預料之外的事件。請細閱本文,並理解我們的實際未來業績或表現可能與預期有重大差異。本文內有關任何董事或本公司意向的陳述或提述乃於本文章刊發日期作出。任何該等意向均可能因未來發展而出現變動。
媒體聯系
Kelly.jiang@[email protected]
18021008361